2 नेमेटल्स बुनियादी रासायनिक तत्व हैं, जिनके परमाणु समान ऊर्जा स्तर के इलेक्ट्रॉनों को स्वीकार करना आसान है, उनके नकारात्मक चार्ज किए गए आयनों को संतुष्ट करते हैं। तत्वों-गैर-फेंकने वाले roztashovanі kіntsі अवधियों में myutnu elektronnuyu कॉन्फ़िगरेशन oznіshny गेंद निकटतम अक्रिय गैस या बराबर के विन्यास के करीब है। लगभग सभी गैर-फेंकने वालों में समान रूप से छोटी त्रिज्या हो सकती है, उनकी विशेषता है उच्च मूल्यइलेक्ट्रोनगेटिविटी और ऑक्साइड पावर।
उदाहरण के लिए, ऐसे समय में जहां प्रोटीन का एक हिस्सा होता है, जिसे हीमोग्लोबिन कहा जाता है, जो एरिथ्रोसाइट्स में मौजूद होता है। Zalіzo vіdpovіdaє chervone farbuvannya के लिए, अगर यह खट्टा जैसा लगता है। प्रकृति में, फर्श के विभिन्न रंगों के हिस्से में बहुत अधिक धातु होती है, उनकी उपस्थिति से डी रंग का संकेत मिलता है। गैर-धातुओं का प्रभुत्व: गैर-धातु, vіdmіnu vіd धातुओं पर, लचीलापन, प्लास्टिसिटी के प्रभुत्व को कम नहीं करते हैं और उनके zdatnosti गर्मी और बिजली का संचालन करते हैं, zahalom, यहां तक कि छोटे; इसके अलावा, धातु की एक परत में बदबू कम मोटी भी हो सकती है।
गैर फेंके गए, इसलिए कोयला, फास्फोरस, सल्फर, सेलेनियम और आयोडीन की तरह, वे अपारदर्शी हैं और कम हो सकते हैं। कोयला, नाइट्रोजन, किसेन, फास्फोरस और सल्फर जैसे गैर-फेंकने वाले डेयाके जीवित जीवों के लिए बहुत महत्वपूर्ण हो सकते हैं, व्यवहार्य प्रोटीन, कार्बोहाइड्रेट, लिपिड और अन्य में उनकी संरचनाओं का एक महत्वपूर्ण हिस्सा बनाने के लिए बदबू के टुकड़े।
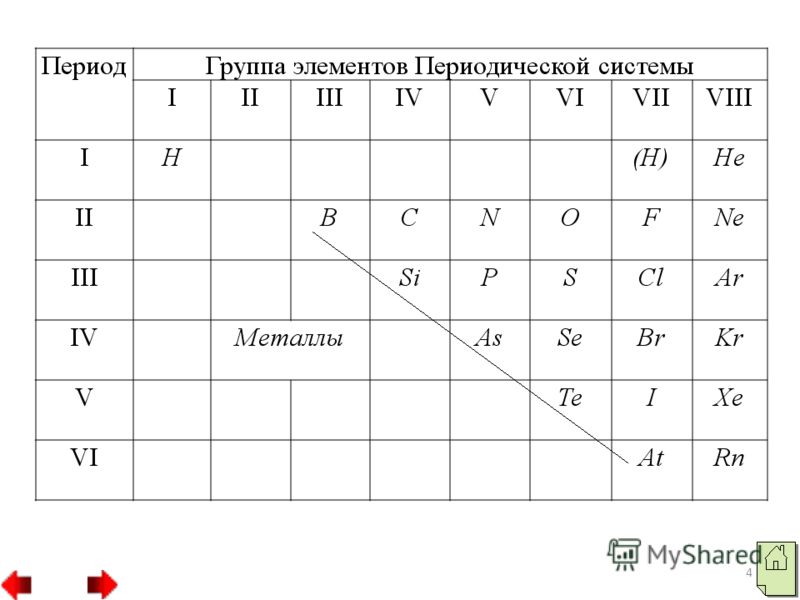
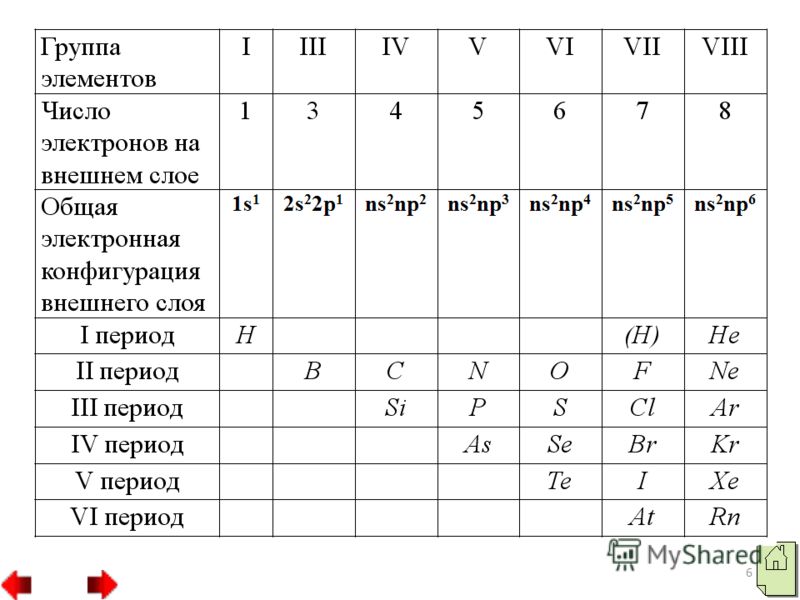
3 मध्य अधातु दो तत्व, जल और हीलियम, s-मातृभूमि की ओर बढ़ते हैं, बाकी सब कुछ p-मातृभूमि में निहित है। बाहरी इलेक्ट्रॉन बॉल पर, गैर-धातुओं के परमाणुओं में इलेक्ट्रॉनों की एक अलग संख्या होती है: पानी के परमाणु में एक इलेक्ट्रॉन (1s") होता है, हीलियम परमाणु में दो इलेक्ट्रॉन होते हैं, बोरॉन परमाणु में तीन इलेक्ट्रॉन होते हैं। गेंदों में बड़ी संख्या हो सकती है। 4 से 8 बजे तक बिजली गैर-ध्रुवीय ध्वनि. बदबू आणविक जीवन को जन्म दे सकती है, जैसे पानी के अणु, खट्टा, नाइट्रोजन और यहां तक कि परमाणु जीवन, जैसे क्रिस्टल से लेकर हीरे या बोरॉन तक।

4
5

6
7
8 प्रकृति में अधातु और योग की भूमिका पहले से ही महान है। नेमेटली मिट्टी के द्रव्यमान का 84%, विकास के द्रव्यमान का 98.5% और लोगों के शरीर के द्रव्यमान का 97.6% हो जाएगा। छह अधातु कोयला, पानी, किसन, नाइट्रोजन, फास्फोरस और सल्फर कार्बनिक तत्व हैं, शार्क प्रोटीन, वसा, कार्बोहाइड्रेट और न्यूक्लिक एसिड के अणुओं के गोदाम में प्रवेश करते हैं। इसे साबित करने के लिए, याकिम मि दीखामो, є सुमेशु सरल और मुड़ा हुआ भाषण, गैर-धातुओं (कीसेन, नाइट्रोजन, कार्बन डाइऑक्साइड) के साथ बनाया गया।

9

10 वाक्-गैर-फेंकने वाले, जो एक आणविक जीवन बना सकते हैं, का उपयोग गैस जैसी, दुर्लभ या ठोस अवस्था में किया जा सकता है। कमजोर अंतर-आणविक बलों के माध्यम से सभी बदबू कम उबलते और पिघलने वाले तापमान से प्रभावित हो सकती है। वाक्-गैर-फेंकने वाले, जो परमाणु हो सकते हैं, केवल एक ठोस समुच्चय अवस्था में पाए जाते हैं, उनके परमाणु अपने स्वयं के सहसंयोजक बंधों से बंधे होते हैं और मैक्रोमोलेक्यूल बनाते हैं, उदाहरण के लिए, Cn, Sn, Sin। उच्च कठोरता, उच्च गलनांक और क्वथनांक की बदबू को ध्वनि दें। बहुत सी गैर-धातु निर्माण सामग्री एलोट्रोपिक संशोधनों में सक्षम हैं: ओ 2, ओ 3. गैर-धातु के लिए गर्मी और इलेक्ट्रिक जेट का संचालन करना अच्छा नहीं है। गैर-धातु क्रिस्टल, गैर-प्लास्टिक और क्रिस्टल। अधिकांश अधातुएँ धातु की चकाचौंध नहीं करती हैं।

11


13


15 गैर-धातुओं के जल ग्रेड को पानी के लिए अलग-अलग सेटिंग्स की विशेषता है। मीथेन और सिलाने पानी में बुरी तरह भिन्न हैं। अमोनिया और फॉस्फीन, जब पानी में घुल जाते हैं, तो कमजोर आधारों को भंग कर देते हैं - अमोनियम हाइड्रॉक्साइड NH 4 OH और फॉस्फोनियम हाइड्रॉक्साइड РH 4 OH। जब पानी को पानी से अलग किया जाता है, सेलेनियम पानी और टेल्यूरिक पानी, साथ ही हलोजन पानी, एसिड और सूत्र स्थापित होते हैं, जो स्वयं पानी होते हैं।

16 बुराई के दायीं ओर की अवधि में, पानी में गैर-धातुओं के गर्मी के पानी की शक्ति की अम्लता बढ़ जाती है, और समूह कमजोर हो जाते हैं। जानवरों के समूहों में पानी की अधातुओं की ऑक्साइड गतिविधि नीचे की ओर बहुत बदल जाती है। एचएफ एचसीएल एचबीआर HI



5. न केवल किसन, बल्कि गैर-धातु (फ्लोरीन, आयोडीन, ब्रोमीन और अन्य) भी तह भाषणों के साथ प्रतिक्रियाओं में ऑक्सीकरण एजेंट की भूमिका निभा सकते हैं। उदाहरण के लिए, एक मजबूत ऑक्सीकरण क्लोरीन, खारा (II) क्लोराइड को खारा (III) क्लोराइड में ऑक्सीकरण करता है:

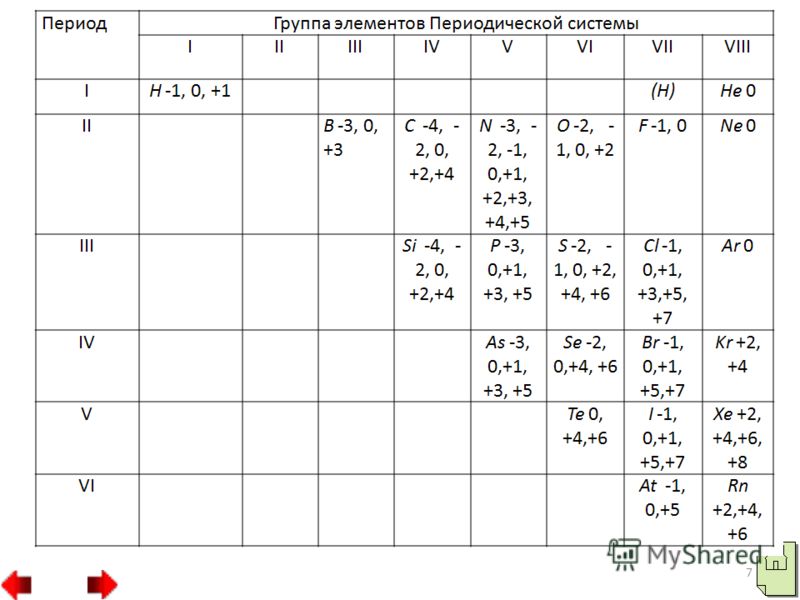
20 फिसलने वाली आवाजें जो फेंकी नहीं (फ्लोरीन के लिए अपराध) शक्ति दिखा सकती हैं और प्रेरित कर सकती हैं। उसी समय, अधातुओं के परमाणु ऑक्सीकरण करने वाले तत्वों के परमाणुओं में स्थानांतरित हो जाते हैं। कोशों में, जो बसे हुए हैं, अधातु परमाणुओं में सकारात्मक ऑक्सीकरण चरण हो सकते हैं। अधातु के ऑक्सीकरण का सबसे सकारात्मक चरण उच्च समूह संख्या की ध्वनि है। गैर-धातुओं की अभिनव गतिविधि:



23 3. कोयले और पानी में शक्ति का सबसे शक्तिशाली प्रभाव डाला जा सकता है: इस रैंक में, व्यावहारिक रूप से सभी डंब ऑक्सीडाइज़र की भूमिका के साथ-साथ खोजकर्ताओं की भूमिका के रूप में कार्य कर सकते हैं। यह देखने लायक है कि आपने किसी तरह के भाषण के साथ इसे फेंका नहीं है।

24 स्व-ऑक्सीकरण-स्व-उपचार (असमानता) की प्रतिक्रियाएं - ये वही प्रतिक्रियाएं हैं, जिनमें एक और एक ही गैर-धातु एक साथ ऑक्सीकरण, और व्यवहार्य है। इसलिए पोखर माध्यमों में फॉस्फोरस, सल्फर, सेलेनियम, क्लोरीन का अनुपातहीन होना: नेमेटल्स, जो पानी में कठोर स्लैब वाले मैट्सनिमी क्रिस्टलीय अनाज (चारकोल, सिलिकॉन) के साथ अप्रभेद्य हैं या पानी (किसन, पानी) में बुरी तरह से अनुपातहीन हैं, अनुपातहीन प्रतिक्रियाओं में भाग नहीं लेते हैं। .

25 गैर-धातु ऑक्साइड दो समूहों में विभाजित हैं: गैर-खारा और नमक बनाने वाले ऑक्साइड। अप करने के लिए गैर खारा ऑक्साइड देखा जाता है: एन 2 ओ, नहीं, सीओ। अधातु ऑक्साइड और लवण बनाने का रेश्टा। अधातुओं के लवण बनाने वाले ऑक्साइड अम्लीय ऑक्साइड में वृद्धि करते हैं। इनमें गैस जैसे (CO2, SO2, NO2), दुर्लभ वाक् (SO3, N2O3) और ठोस (P2O5, SiO2) शामिल हैं। एसिड ऑक्साइड - एसिड के एनहाइड्राइड्स। उदाहरण के लिए: सीओ 2 - कार्बोनिक एसिड एच 2 सीओ 3 का एनहाइड्राइड; पी 2 ओ 5 - निर्जल फॉस्फोरिक एसिड एच 3 पीओ 4।

26 पशु के सिर के उपसमूहों में, अधिक गैर-धातु आक्साइड की अम्लीय शक्ति नीचे की ओर कम हो जाती है, और अवधियों में, अम्लीय शक्ति दाईं ओर बढ़ जाती है: पानी में SiO 2 P 2 O 5 SO 3 Cl 2 O 7, हाइड्रेटिंग ऑक्साइड, याक अपने चरित्र के लिए - एसिड:

27
28
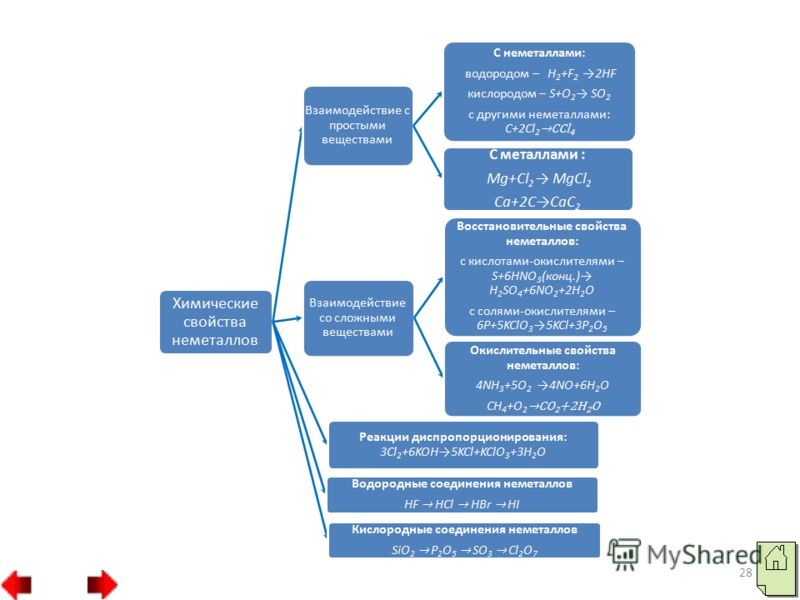


31 2. देयाके नेमेटल को प्रेरणा से दूर किया जा सकता है। उदाहरण के लिए, फास्फोरस, मिश्याक, सुरमा और विस्मुथ कोयले से दूर ले जाते हैं: 3. भौतिक तरीके: ए) कम तापमान आसवन - इस प्रकार समय-समय पर खट्टा प्राप्त होता है; बी) गहरी शीतलन और वाष्पीकरण - इसलिए वे बार-बार नाइट्रोजन प्राप्त करते हैं

32
33 पोषण 1. आवर्त प्रणाली के कुछ समूहों और अवधियों में रासायनिक तत्वडी.आई. 2. गैर-फेंकने वाले परमाणु क्रिस्टल जाली कैसे बनाते हैं, आणविक कैसे होते हैं और वे कुछ परमाणुओं में कैसे पाए जा सकते हैं? 3. 20 डिग्री सेल्सियस पर किस प्रकार का अधातु दुर्लभ है, अधातु - गैस और याक - कठोर भाषण क्या है? 4. डी.आई. की सारणियों में तत्वों के अधातु अभिलक्षण कैसे बदलते हैं?

34 5. बताएं कि कौन से तत्व ऑक्सीकृत होते हैं और जो प्रतिक्रियाओं में समान होते हैं सरल भाषण: ए) एस + ओ 2 \u003d एसओ 2; बी) एस + 2 सीएल 2 = एससीएल 4; सी) सीएल 2 + एच 2 = 2 एचसीएल; डी) 2पी + 3बीआर 2 = 2पीबीआर आगामी प्रतिक्रियाओं के समीकरण को संग्रहीत करना: ए) सी + एच 2 एसओ 4 (संक्षिप्त) \u003d बी) सी + एचएनओ 3 (संक्षिप्त) \u003d सी) एस + एचएनओ 3 (संक्षिप्त) \u003d

बुडोवा और सरल भाषणों की शक्ति अधातु है।
सबसे बड़े प्रकार के गैर-धातु आणविक हो सकते हैं, और सबसे छोटे प्रकार गैर-आणविक होते हैं। सिम करें और उनके अधिकारियों की शक्ति की व्याख्या करें। मूल रूप से योजना 2 में दिखाया गया है। गैर-आणविक नवोदित और आणविक बडिंग के साथ सरल भाषण C, B, SiF2, O2, Cl2, Br2, N2, I2, S8 उच्च तापमानपिघलना इन अधातुओं में ठोस अवस्था में आणविक क्रिस्टलीय दाने होते हैं।
पर मनत्से गैसी, रिदिनी या कठिन भाषण z कम तामपानपिघलना तालिका 2 क्रिस्टल बीर याक और क्रिस्टल सिलिकॉन पानी 2075C के उच्च गलनांक और महान कठोरता के साथ। तापमान परिवर्तन के साथ जंगल की विद्युत चालकता बहुत बढ़ जाती है, जिससे हीटिंग उपकरण को व्यापक रूप से स्थापित करना संभव हो जाता है। स्टील और एल्युमिनियम, मिडी, निकेल और अन्य मिश्र धातुओं में बोरॉन मिलाना। उनकी यांत्रिक शक्तियों में सुधार।
डीकिम धातुओं के साथ बोरिडी बोरॉन, उदाहरण के लिए टाइटेनियम TiB, TiB2 जेट इंजन के पुर्जे, गैस टरबाइन ब्लेड की तैयारी के लिए आवश्यक हैं। जैसा कि योजना 2 से देखा जा सकता है, कोयला सी, सिलिकॉन सी, बोरॉन एक जीवन की तरह हो सकता है और कुछ जंगली शक्तियों से भरा हो सकता है। भाषण जितना सरल, दो प्रजातियों में बदबू आती है, एक क्रिस्टलीय और एक अनाकार। उच्च गलनांक के साथ इन तत्वों की क्रिस्टलीय प्रजातियां पहले से ही ठोस हैं। क्रिस्टलीय सिलिकॉन शक्ति का संवाहक हो सकता है।
सभी तत्व धातु कार्बाइड, सिलसाइड और बोराइड CaC2, Al4C3, Fe3C, Mg2Si, TiB, TiB2 के साथ मिश्रित होते हैं। Deyakі z उन्हें अधिक कठोरता दे सकता है, उदाहरण के लिए Fe3C, TiB। कैल्शियम कार्बाइड को एसिटिलीन में बदल दिया जाता है। जहां तक फ्लोरीन, क्लोरीन और अन्य हैलोजन के परमाणुओं में ऑर्बिटल्स के पीछे इलेक्ट्रॉनों के वितरण की बात है, तो उनकी प्रमुख शक्तियों के बारे में अंदाजा लगाया जा सकता है। फ्लुओरीन परमाणु का कोई मुक्त कक्षक नहीं होता है। वह फ्लोरीन परमाणु अधिक संयोजकता I और ऑक्सीकरण चरण 1 दिखा सकता है। अन्य हैलोजन के परमाणुओं में, उदाहरण के लिए, क्लोरीन परमाणुओं में, समान ऊर्जा स्तर पर, d-कक्षक होते हैं।
Zavdyaki tsyom rozparyuvannya elektronіv तीन अलग-अलग रास्ते हो सकते हैं। पहले चरण में, क्लोरीन ऑक्सीकरण चरण 3 दिखा सकता है और क्लोराइड एसिड HClO2 को भंग कर सकता है, जिसका उपयोग क्लोराइट के लवण द्वारा किया जाता है, उदाहरण के लिए, पोटेशियम क्लोराइट KClO2। एक अन्य मामले में, क्लोरीन ऑक्सीकरण के कुछ चरणों में क्लोरीन 5 में घुल सकता है। क्लोरोवेट एसिड HClO3 और क्लोरेट के її लवण, उदाहरण के लिए पोटेशियम क्लोरेट KClO3, बर्थोलेट की सिल। तीसरे चरण में, क्लोरीन ऑक्सीकरण अवस्था 7 प्रदर्शित करता है, उदाहरण के लिए, परक्लोरिक एसिड HClO4 में और परक्लोरेट लवण में, उदाहरण के लिए, पोटेशियम परक्लोरेट KClO4 में। 4. किसनेवो और पानीदार अधातु।
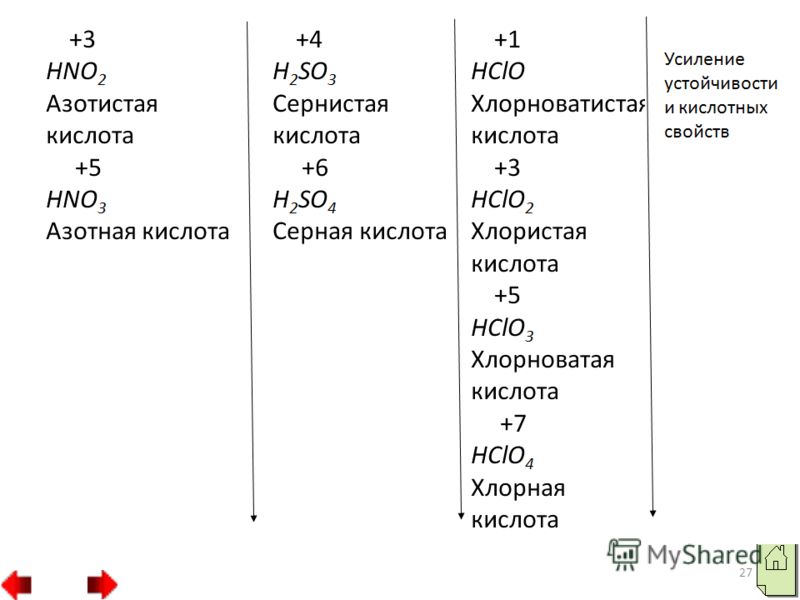
उनकी शक्तियों का संक्षिप्त विवरण। खट्टे के साथ, गैर-धातुएं एसिड ऑक्साइड को भंग कर देती हैं। कुछ ऑक्साइड में, बदबू अधिकतम ऑक्सीकरण अवस्था दिखाती है, जो समूह की संख्या के बराबर होती है, उदाहरण के लिए, SO2, N2O5, और अन्य में, निचला वाला, उदाहरण के लिए, SO2, N2O3। एसिड ऑक्साइड को एसिड दिया जाता है, इसके अलावा, एक गैर-धातु के दो अम्लीय एसिड दूसरे की तुलना में अधिक मजबूत होते हैं, जिसमें वाइन यह उच्च स्तर का ऑक्सीकरण दिखाता है।
उदाहरण के लिए, नाइट्रिक एसिड HNO3 नाइट्रोजनस HNO2 से अधिक मजबूत है, और सल्फ्यूरिक एसिड H2SO4 सल्फ्यूरिक एसिड H2SO3 से अधिक मजबूत है। गैर-धातुओं की अम्लता के संकेत 1. टोबटो के वर्तमान ऑक्साइड की शक्ति। ऑक्साइड, गोदाम से पहले जिसमें इस समूह का तत्व शामिल है, दायीं ओर बढ़ने की अवधि में उच्च स्तर के ऑक्सीकरण के साथ, मूल से अम्लीय में चरणबद्ध परिवर्तन। 2. जन्तुओं के समूहों में, अधिक से अधिक ऑक्साइड की अम्ल शक्ति धीरे-धीरे नीचे तक कमजोर हो जाती है।
एसिड के प्रभुत्व से न्याय करना संभव है, जो उनके आक्साइड के समान है। 3. बुराई की अवधि में उच्च तत्वों के उच्च ऑक्साइड की एसिड शक्ति की वृद्धि को इन तत्वों के आयनों के सकारात्मक चार्ज की चरणबद्ध वृद्धि द्वारा समझाया गया है। 4. रासायनिक तत्वों के आवर्त तंत्र के मुख्य उपसमूहों में अधातुओं के बड़े ऑक्साइडों की अम्लीय शक्ति नीचे से नीचे की ओर बदलती रहती है।
रासायनिक तत्वों की आवधिक प्रणाली के समूहों के बाद के जल दिनों के वैश्विक सूत्र तालिका 3 में अनुमानित हैं। IVVVIVIIRHRH2RH3RH4RH3H2RHR समूहों के पीछे के क्षेत्रों के वैश्विक सूत्र इसलिए इनका गलनांक अधिक होता है।
गैर-धातुओं के साथ, पानी आणविक जीवन के आधे से वर्षों को भर देता है। सबसे बड़े दिमागों में ची ची लेटकी रेडिनी होती है। गर्मी के पानी की शक्ति की हल्की अम्लता की अवधि में, पानी में अधातुएँ गुलाब हो जाती हैं। हम सराहना करते हैं कि वे इलेक्ट्रॉनिक दांव में खट्टे हैं, और वे कक्षीय में पानी में हैं, एक प्रक्रिया है जो इस तरह दिखती है H2O HF H3O F एसिड पावर दिखा रहा है।
इस प्रक्रिया के लिए, वातावरण खट्टा होता है और इलेक्ट्रॉन जोड़ी से मेल नहीं खा सकता है, और आयन पानी एक मुक्त कक्षीय है, जिसके लिए दाता-स्वीकर्ता लिंक स्थापित होता है। जब पीने के पानी से अमोनिया छोड़ा जाता है, तो प्रजनन प्रक्रिया होती है। और नाइट्रोजन के टुकड़े एक असंगत इलेक्ट्रॉन जोड़ी दे सकते हैं, और वे एक पानीदार कक्षीय बनाते हैं, एक योजक कनेक्शन बनाते हैं, और वे अमोनियम एनएच 4 और हाइड्रॉक्साइड-आयनों में बस जाएंगे।
इस प्रक्रिया को सूत्र H2O NH3 NH4 OH . द्वारा व्यक्त किया जा सकता है अमोनिया मुख्य शक्ति को दर्शाता है। अब देखते हैं क्यों जल डेफ्लोरीन, हाइड्रोजन फ्लोराइड पानी में एचएफ, एसिड, कमजोर एले, कम क्लोरीन। हम ध्यान दें कि फ्लोरीन में आयनों की त्रिज्या क्लोरीन में आयनों की तुलना में काफी कम है। इसलिए, फ्लोरीन पानी को आकर्षित करने में अधिक समृद्ध है, कम क्लोरीन।
सीआईएम के साथ बंधन में, हाइड्रोफ्लोरिक एसिड का पृथक्करण हाइड्रोक्लोरिक एसिड, टोबो की तुलना में काफी कम है। हाइड्रोफ्लोरिक एसिड हाइड्रोक्लोरिक एसिड से कमजोर है। लक्ष्य बटों के साथ, आप इतनी मेहनत कर सकते हैं
केनेट्स रोबोटी -
इस विषय को विभाजित किया जाना चाहिए:
नेमेटली
विभिन्न ऐतिहासिक युगों में, तत्व की समझ को एक अलग ज़मिस्ट में निवेश किया गया था। प्राचीन यूनानी दार्शनिकों ने, तत्वों की तरह, चोतिरी को देखा ... मध्य युग में, ताकत, वह पारा, इन कोबों तक पहुंच गया। 17वीं शताब्दी में आर. ... समय बीतने के साथ कई मुड़े हुए भाषण टेबल पर पहुंच गए थे। डेनमार्क में, समझने का समय रासायनिक है।
यदि आपको इस विषय पर पूरक सामग्री की आवश्यकता है, अन्यथा आप मजाक करने वालों को नहीं जानते हैं, तो यह अनुशंसा की जाती है कि आप हमारे आधार को रॉबिट द्वारा खोजें:
छीनी गई सामग्री के साथ रॉबिटिमो क्या है:
यदि यह सामग्री आपको परिचित लगती है, तो आप इसे सामाजिक उपायों में अपने पक्ष में सहेज सकते हैं:
